本翻譯僅作學術交流用,無商業意圖,請勿轉載,如有疑議問請來信
英國一項長達8年的研究發現,低碳水化合物飲食和體重控制能顯著提高2型糖尿病患者達到無藥物治療緩解的機會。研究涵蓋9800名患者,其中51%實現了疾病緩解。此外,該方法對於新診斷的糖尿病患者特別有效,並為健康管理和醫療成本節約提供了新的思路。

無藥物治療型2糖尿病復原的預測因素?從一項8年期全科醫療服務評估低碳水化合物飲食與減重的洞察
What predicts drug-free type 2 diabetes remission? Insights from an 8-year general practice service evaluation of a lower carbohydrate diet with weight loss
Unwin D, Delon C, Unwin J, et alWhat predicts drug-free type 2 diabetes remission? Insights from an 8-year general practice service evaluation of a lower carbohydrate diet with weight lossBMJ Nutrition, Prevention & Health 2023;6:doi: 10.1136/bmjnph-2022-000544
https://nutrition.bmj.com/content/6/1/46
Abstract
Background
Type 2 diabetes (T2D) is often regarded as a progressive, lifelong disease requiring an increasing number of drugs. Sustained remission of T2D is now well established, but is not yet routinely practised. Norwood surgery has used a low-carbohydrate programme aiming to achieve remission since 2013.
Methods
Advice on a lower carbohydrate diet and weight loss was offered routinely to people with T2D between 2013 and 2021, in a suburban practice with 9800 patients. Conventional ‘one-to-one’ GP consultations were used, supplemented by group consultations and personal phone calls as necessary. Those interested in participating were computer coded for ongoing audit to compare ‘baseline’ with ‘latest follow-up’ for relevant parameters.
Results
The cohort who chose the low-carbohydrate approach (n=186) equalled 39% of the practice T2D register. After an average of 33 months median (IQR) weight fell from 97 (84–109) to 86 (76–99) kg, giving a mean (SD) weight loss of −10 (8.9)kg. Median (IQR) HbA1c fell from 63 (54–80) to 46 (42–53) mmol/mol. Remission of diabetes was achieved in 77% with T2D duration less than 1 year, falling to 20% for duration greater than 15 years. Overall, remission was achieved in 51% of the cohort. Mean LDL cholesterol decreased by 0.5 mmol/L, mean triglyceride by 0.9 mmol/L and mean systolic blood pressure by 12 mm Hg. There were major prescribing savings; average Norwood surgery spend was £4.94 per patient per year on drugs for diabetes compared with £11.30 for local practices. In the year ending January 2022, Norwood surgery spent £68 353 per year less than the area average.
Conclusions
A practical primary care-based method to achieve remission of T2D is described. A low-carbohydrate diet-based approach was able to achieve major weight loss with substantial health and financial benefit. It resulted in 20% of the entire practice T2D population achieving remission. It appears that T2D duration <1 year represents an important window of opportunity for achieving drug-free remission of diabetes. The approach can also give hope to those with poorly controlled T2D who may not achieve remission, this group had the greatest improvements in diabetic control as represented by HbA1c.
摘要
背景
2型糖尿病(T2D)通常被視為一種需要越來越多藥物治療的持續性、終身性疾病。 T2D的持續性緩解現已充分確認,但尚未成為常規實踐。 諾伍德診所自2013年起使用低碳水化合物計劃,旨在實現疾病緩解。
方法
2013年至2021年間,該郊區診所向9,800名患者中的第二型糖尿病患者常規提供低碳水化合物飲食和減重建議。 使用傳統的「一對一」全科醫生諮詢,必要時輔以團體諮詢和個人電話回訪。 對有興趣參與的患者進行電腦編碼,以便持續審計,比較「基線」與「最新追蹤」的相關參數。
结果
選擇低碳水化合物方法的隊列(n=186)佔該診所2型糖尿病登記冊的39%。 平均33個月後,中位數(四分位數間距)體重從97(84-109)公斤下降至86(76-99)公斤,平均(標準差)體重減輕−10(8.9)公斤。 中位數(四分位數間距)HbA1c從63(54-80)mmol/mol下降至46(42-53)mmol/mol。 77%患病不到1年的T2D患者實現了糖尿病緩解,而患病時間超過15年的患者緩解比率降至20%。 整體而言,該隊列有51%實現了疾病緩解。 平均低密度脂蛋白膽固醇降低了0.5 mmol/L,平均三酸甘油酯降低了0.9 mmol/L,平均收縮壓降低了12毫米汞柱。 藥物開支大幅減少;諾伍德診所每年每位糖尿病患者的藥物開支平均為4.94英鎊,而本地其他診所為11.30英鎊。 截至2022年1月的一年中,諾伍德診所比地區平均每年節省68,353英鎊。
結論
描述了一種實用的基層醫療方法,用於達到第2型糖尿病的緩解。 基於低碳水化合物飲食的方法能夠實現顯著的體重減輕,並帶來重大的健康和經濟效益。 它使得整個診所2型糖尿病人群中20%實現了緩解。 病程<1年似乎是實現無藥物糖尿病緩解的重要機會窗口。 這種方法也為那些控制不良的第二型糖尿病患者帶來希望,即使他們可能無法實現緩解,這一組人在糖尿病控制方面的改善(以HbA1c表示)最為顯著。
引言
2021年,英國營養學會發表了一篇關於不用藥物治療2型糖尿病(T2D)的飲食策略回顧,其中指出「全面飲食替代和低碳水化合物飲食已被證明有效促進體重減輕和T2D緩解」。然而,對於使用低碳水化合物飲食達到體重減輕或糖尿病緩解的焦點,後續的綜合分析並不總是支持。有必要對這種方法的成效進行實際數據上的研究,並探討哪些臨床方面有助於其成功。
在本文中,我們檢視了2013年至2021年間,英國一家初級保健診所為T2D患者提供低碳水化合物治療方法的真實世界數據。飲食減重引起緩解的生理機制首次在2011年得到證明。自那以後,不用藥物治療T2D的理念獲得了國際上的關注。我們現在有了一個關於緩解的國際共識:糖化血紅蛋白(HbA1c)<48毫摩/升,持續3個月以上,且無需使用糖尿病藥物。早期的實踐審計顯示:HbA1c、血脂和血壓(儘管減少了20%的抗高血壓藥物處方)有顯著改善,腎功能和肝功能也有所提升。不僅顯示了重大的健康改善,還節省了大量的藥物預算。
我們對8年數據集的分析探討了哪些因素預測緩解,其持久性以及那些未達到緩解的患者的血糖控制情況。
方法
自2013年3月起,我們由九名特別訓練的全科醫生和三名執業護士組成的團隊,向T2D患者(定義為兩次檢測HbA1c >48毫摩/升)提供降低飲食中碳水化合物的建議(線上補充文件1,低碳水化合物方案)。我們的方案包括圍繞降低血壓和T2D藥物處方的重要信息;發現血壓和血糖通常會改善到需要藥物審查的程度。首先檢查和討論體重是每次諮詢的第一步,然後提供低碳水化合物飲食作為一種選擇,並簡單明了地解釋關鍵生理原理,強調:良好的糖尿病控制是關於避免血糖高峰所造成的損害,「時間範圍」很重要,高血糖通常反映了最近所吃食物,不同食物會對血糖和胰島素水平產生不同的反應,澱粉性碳水化合物包含許多葡萄糖分子,導致顯著的血糖升高,以及減重是過程的一部分。(線上補充文件2)。
我們將高血糖視為一個有趣的謎題而非問題,與患者一起探索解決方案。在一些案例中,患者最初有所改善後,體重或HbA1c開始上升,我們早期觀察到,大多數患者實際上增加了他們的碳水化合物攝入量(碳水化合物潛移)。通常,一通簡短的電話就能激勵他們做出改變。
我們的許多經驗較少的臨床醫生擔心討論肥胖可能被視為「羞辱肥胖」。我們鼓勵他們解釋減重真的有助於人們的健康,並詢問他們是否有興趣合作達成這一目標。通過這種方式,我們提供了相關信息,然後在提供更具體建議之前確認對方是否願意進行。
對於選擇低碳水化合物計劃的患者,我們在常規全科醫生或執業護士諮詢中,確定基線體重和血液結果並給予飲食建議。每次訪問都會測量體重,根據患者選擇和臨床需求量身定制持續支持的程度。除了10分鐘的「一對一」預約(我們估計每位患者每年平均有三次諮詢)外,該診所還提供可選的90分鐘晚間小組會議,大約每6週一次。小組會議邀請患者的家屬參加,因為一些患者依賴他人購買食物或烹飪。小組會議為人們提供了互相實際支持的場所,並培訓新員工。每次會議平均有25位患者參加。自COVID-19大流行開始以來,這些小組會議以Zoom線上會議的形式舉行。這使我們能夠向診所中所有T2D患者發送會議連結,邀請他們參加。這對於那些希望進行「複習」的患者特別重要。
我們製作了教育資源來支持患者和員工。低碳水化合物飲食單(線上補充文件3)概述了合適的食物來源。我們還提供了血糖負荷數據,以鼓勵減少攝入含糖和澱粉食品。例如,用全脂乳製品、雞蛋、綠葉蔬菜、肉類、魚類、漿果和堅果(考慮到每位患者的社會文化飲食需求和偏好)來替代早餐穀物、大米、麵包和馬鈴薯。從2018年起,員工培訓通過完成一位作者編寫的英國全科醫生學院關於T2D和血糖指數的網上學習模塊正式化。
這篇文章是對服務提供的持續審計的一部分。這是一個循環過程,需要定期更新方案,並基於此類審計在全院分享「有效之處」。因此,自2013年以來,我們的方法有所改進。結果在初期表現出色後有所下降的趨勢,促使我們專注於有效維持飲食變化。我們建議患者預見假期、聖誕節和生日等挑戰,這些時刻往往是許多飲食失敗的時候。我們鼓勵患者注意這些時期的體重增加並採取行動。計算機生成的所有測量指標的圖表以患者反饋的形式發送(接待人員稱這為「快樂郵件」)。大約在2016年,我們意識到導致患者重新增重的另一個可能的行為因素:「食物成癮」。為此,我們支持患者識別並完全避免他們的「觸發食物」。
通過鼓勵參與者考慮他們的個人希望和健康目標,可用的資源,設定現實的下一步行動,並使個人注意到對他們有效的事物,我們實現了進一步的行為改變(線上補充文件4)。我們會強調無藥物緩解帶給T2D患者的希望的力量。這種模式對於維持我們臨床團隊的動力和幫助其發展至關重要。最後,在行為改變方面,我們學會了詢問人們最佳學習方式:他們是偏好傳單、書籍還是應用程序?
排除標準包括嚴重精神疾病、晚期疾病和飲食失調。
常規臨床數據從2013年3月到2021年4月收集。在手術中進行體重和血壓的基線測量,並由當地NHS抽血診所進行血液測試(HbA1c、脂質檔案)。血液檢測的頻率取決於臨床需求和風險評估,作為標準護理的一部分。一些患者發現將禁食血液檢查融入他們的生活方式模式很有挑戰性,因此我們的結果包含了更多脂質檔案不完整數據集,而不是其他測量。
統計分析是使用R V.4.0.2進行的。基線和後續數據的總結以年齡、體重、HbA1c、脂質檔案和血壓等非正態分佈連續變量的中位數和四分位距(IQR,25百分位數,75百分位數)顯示。更正常分佈的連續變量,如飲食持續時間,以平均值(SD)呈現。使用Wilcoxon符號排名檢驗配對樣本,對基線和最新後續連續變量進行比較。p<0.05被認為是統計上顯著的。
基線和最新後續數據分佈以盒鬚圖呈現,盒子代表中位數和IQR,紅點表示平均值,上下鬚鬚表示最小/最大值,或1.5倍的IQR。
線性回歸模型以HbA1c減少作為結果,以基線HbA1c作為預測因子。使用緩解發生作為結果,以性別、基線年齡、基線體重、基線HbA1c和T2D持續時間作為預測因子的邏輯回歸模型。
結果
在8年的時間內(2013年3月至2021年4月),Norwood診所的2型糖尿病病例登記共有473人,其中186人(39%)選擇了低碳水化合物方法。在這些人中,114人(61%)是男性,基線時的中位數(IQR)年齡為63(54,73)歲。隨訪平均(SD)持續時間為33(27)個月。37.6%的病例組是診斷後1年內的患者。
對於整個開始低碳水化合物計劃的病例組,中位數(IQR)體重從97(84-109)公斤降至86(76-99)公斤,平均(SD)體重減輕為-10(8.9)公斤;p<0.001。中位數(IQR)HbA1c從63(54-80)毫摩/升降至46(42-53)毫摩/升;p<0.001。中位數(IQR)甘油三酯從2.1(1.4-3.2)毫摩/升降至1.4(1.0-1.9)毫摩/升;p<0.001。中位數(IQR)收縮壓從140(134-150)毫米汞柱降至132(122-138)毫米汞柱;p<0.001。中位數(IQR)總膽固醇從4.9(4.1-5.7)毫摩/升降至4.3(3.6-5.0)毫摩/升;p<0.001。中位數(IQR)總膽固醇與高密度脂蛋白(HDL)比值從4.0(3.0-5.0)降至3.9(3.0-4.4);p<0.001(表1,圖1和線上補充文件5)。
表1比較186位接受低碳水化合物飲食建議的2型糖尿病患者的基線和最新後續數據,並將其分為兩個子組;94位達到緩解的患者和92位未達到緩解的患者。
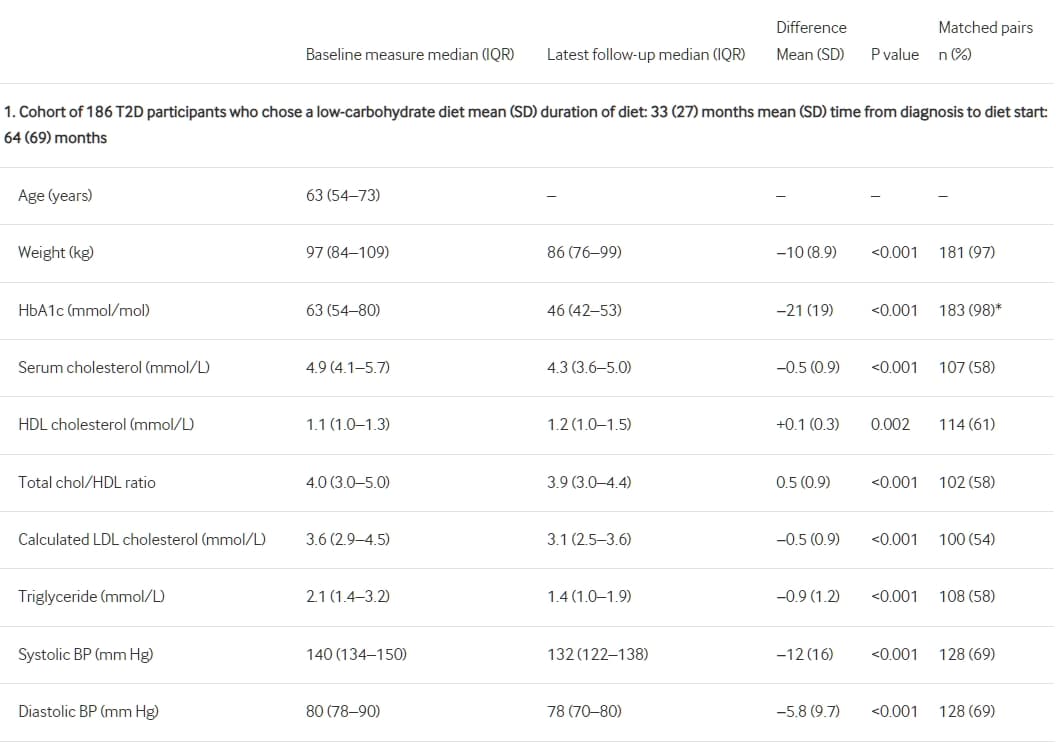
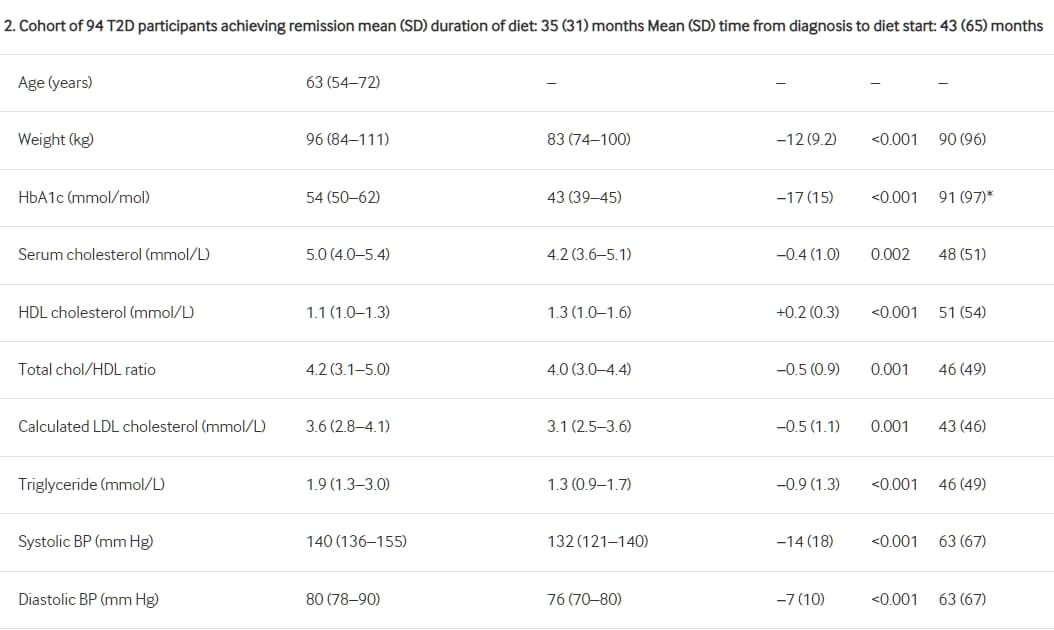
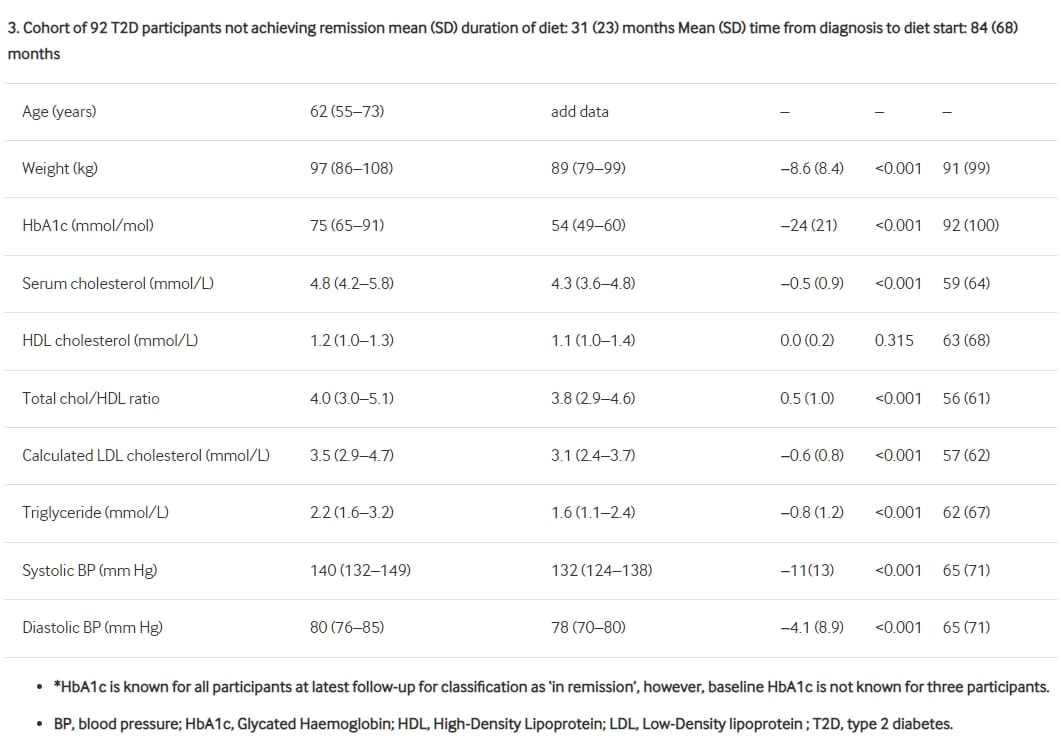
追蹤平均33個月的186位2型糖尿病患者的體重、代謝參數和收縮壓變化。BP,血壓;T2D,2型糖尿病。HDL,高密度脂蛋白。
基線和最新後續數據的緩解和非緩解子群體進一步在表1中進行比較。緩解組的平均(SD)體重變化為-12(9.2)公斤,與非緩解組的-8.6(8.4)公斤相比(無顯著差異)。沒有患者在不減重的情況下達到緩解,儘管在三名患者中減重為1公斤或更少。緩解和非緩解組之間體重變化的分佈顯示在圖2中。在緩解組中,HbA1C平均(SD)下降了17(15)毫摩/升,而非緩解組則為24(21)毫摩/升。緩解組的基線HbA1c也較低(圖3和表2)。這組人均(SD)遵循飲食37(42)個月,而非緩解組為31(23)個月。
圖2將患者分為達到緩解和未達到緩解的兩組,並根據體重變化(以公斤計)進行繪圖。NA,不適用。
圖3基線和最新後續的HbA1c數據(以毫摩/升計)分為緩解和無緩解組,以盒鬚圖顯示。低碳水化合物飲食的平均持續時間為33個月。HbA1c,糖化血紅蛋白。
表2比較186位選擇低碳水化合物飲食的2型糖尿病患者群體的基線數據,分為:(1)達到緩解的群體;(2)未達到緩解的群體。
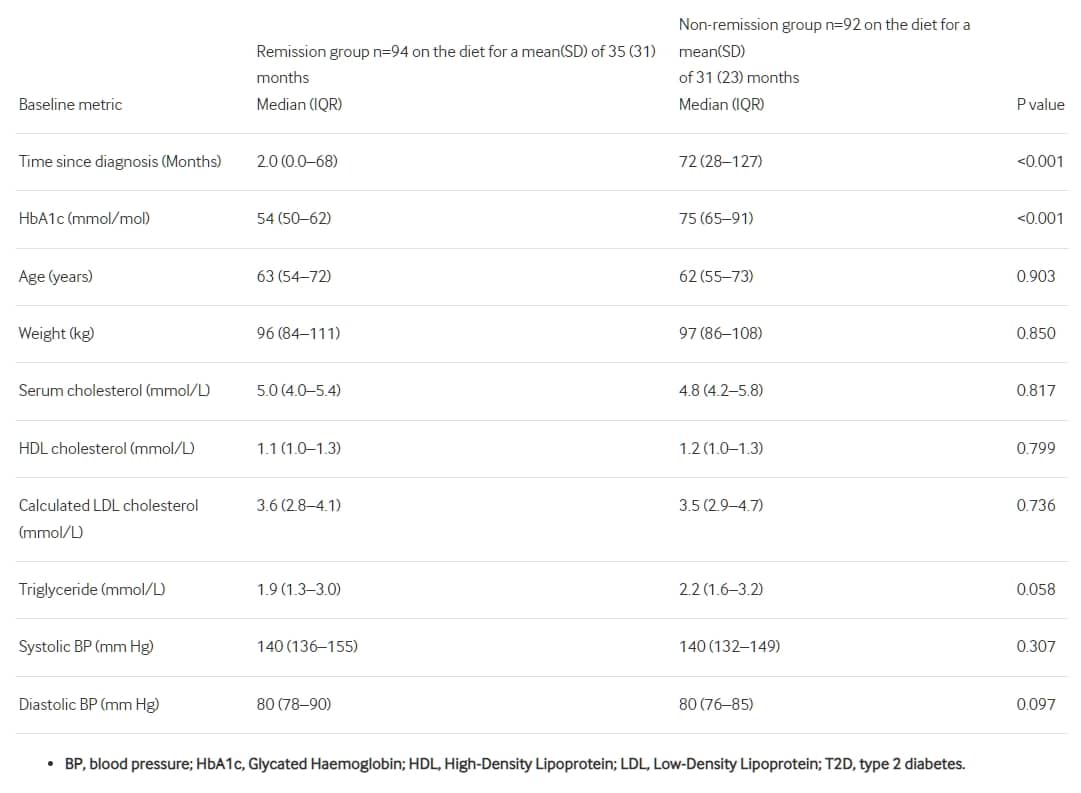
表2顯示了緩解組與非緩解組基線數據的比較。只有兩個指標顯示顯著差異:緩解組的基線中位數(IQR)HbA1c為54(50-62)毫摩/升,與非緩解組的75(65-91)毫摩/升相比(p<0.001)。診斷後時間的基線中位數(IQR)對於緩解組為2(0.0-68)個月,而對於非緩解組為72(28-127)個月(p<0.001)。緩解組更有可能是最近被診斷,並且有顯著較低的基線HbA1c。所有其他基線指標:年齡、體重、血脂和血壓在緩解和非緩解組之間沒有顯著差異。
一個以HbA1c減少為結果,以基線HbA1C為預測因子的線性回歸模型顯示了一個高度顯著的關係R2=0.74; p<0.0001(圖4和線上補充文件6)。開始時HbA1c最高的人更有可能在HbA1c上取得最大的改善,但達到緩解的可能性較低(邏輯回歸,線上補充文件7)。圖4還顯示,178名患者的HbA1c有所改善,僅有5人(3%)在最新的後續檢查中結果更差。
圖4關於基線HbA1c的33個月平均HbA1c改善的回歸分析。HbA1c,糖化血紅蛋白。
糖尿病的近期診斷(<1年)是緩解的重要預測因子(見圖5,線上補充文件7)。在診斷後的第一年內,77%接受低碳水化合物建議的人在不使用任何糖尿病藥物的情況下達到了HbA1c<48毫摩/升。對於已確立的T2D,持續1-5年、5-10年、10-15年和超過15年的比例分別為35%、31%、44%和20%。到2021年4月,共有94人達到了緩解,這佔選擇低碳水化合物方法的人數的51%,以及整個診所T2D病例登記的20%(表3)。
圖5一個由186位2型糖尿病患者組成的群體,平均遵循低碳水化合物飲食33個月,根據診斷後的年數進行分層,比較緩解組(94人)和非緩解組(92人)在2型糖尿病診斷後時間的基線數據。T2D,2型糖尿病。
表3Norwood診所關於2型糖尿病緩解的數據(2015年3月至2021年4月)
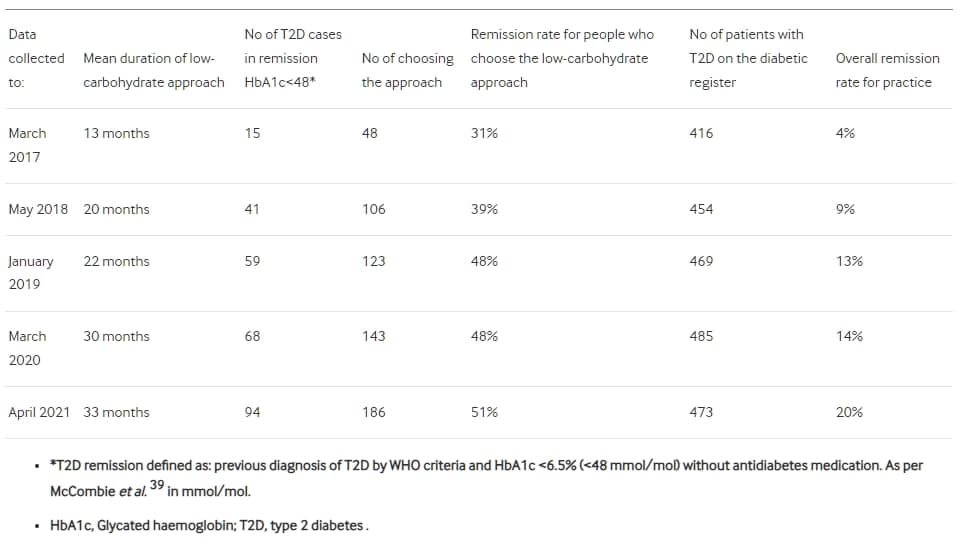
使用邏輯回歸模型預測緩解,查看基線HbA1c、體重、年齡、性別和診斷後時間的數據(線上補充文件9和10),顯示只有較低的基線HbA1c和較短的2型糖尿病診斷後時間是緩解的良好預測因子。這兩個因素綜合起來可以預測緩解的準確性(95%CI)為79%(72%至84%),靈敏度為73%,特異性為85%。
查閱截至2022年1月的一年內Openprescribing網站的數據顯示,組成Southport和Formby臨床委員會的16家當地全科醫生診所中,Norwood診所在糖尿病藥物上的支出比本地區平均水平低68,353英鎊(線上補充文件11)。
討論
在我們的186名患者中,他們平均遵循低碳水化合物計劃33個月,平均體重下降了10公斤,HbA1c下降了21毫摩/升,低密度脂蛋白(LDL)膽固醇、甘油三酯、收縮壓和舒張壓顯著減少。高密度脂蛋白膽固醇顯著增加。這些因素是2型糖尿病和心血管疾病的主要風險因素之一。51%的病例組達到了2型糖尿病緩解,佔診所2型糖尿病病例登記的20%。
這些結果與許多低碳水化合物飲食研究報告的結果非常不同,必須考慮其原因。顯著的觀察是體重的大幅下降,這在這種飲食方法的研究中並不總是看到的。體重減輕觀察到的唯一其他低碳水化合物飲食研究也實現了良好的2型糖尿病緩解率。由受信任的健康專業人員提供指導和坦誠討論減重的重要性似乎在帶來觀察到的效果方面很重要。一線保健團隊實現了一貫的長期管理。
持續的支持對於防止回歸舊習慣至關重要。對於某些人來說,食物可能就像尼古丁和酒精一樣上癮。這可能解釋為什麼高度加工的食物如此難以永久放棄。我們發現食物成癮的概念可以幫助人們更好地理解他們與食物的關係。這種方法的持續效益取決於堅持飲食和長期減重。我們的一位患者評論說「這是一種生活方式而不僅是飲食」。我們的計劃專注於飲食,加入運動可能會進一步改善結果。該計劃的重要部分是持續監測體重,以便及早發現「重新滑落」。對於大多數人來說,體重增加和HbA1c的上升僅僅是「碳水化合物潛移」的反映,臨床醫生應該認識到這一點。這並不是飲食本身失敗,而是飲食遵循失敗。對於許多人來說,這種情況只需要打個電話詢問「您有什麼想法為什麼您的血變得更甜嗎?」這種親密的個人後續觀察到是有效的。我們發現大多數人知道碳水化合物已經悄悄回來,並意識到他們需要回到之前有效的方法。這就是我們通過Zoom進行開放式小組工作的地方。那些需要複習的人可以不用預約就加入。我們很少看到HbA1c上升儘管體重顯著減輕的令人擔憂的情況。顯然應該考慮到1型糖尿病或胰腺癌的漏診。我們還學會了提前預測並討論像聖誕節和假期這樣的挑戰情況,有助於我們的患者在問題出現之前進行計劃。對於許多控制失敗的人,我們發現詢問「下次您能做些什麼不同?」很有幫助。憑藉同理心和持續的支持,我們的錯誤可以成為學習的機會。
我們成功的重要組成部分似乎是在支持人們考慮2型糖尿病不同方法的同時提供希望。對於那些長期患有2型糖尿病且糖尿病控制不良的人來說,激發他們的熱情似乎是一個挑戰。然而,先前的質性研究表明,將飲食方法用於管理糖尿病是被廣泛接受的,特別是在患有2型糖尿病多達6年的人群中。儘管我們發現長期患有2型糖尿病的人緩解率較低,但這一高風險群體仍然從降低碳水化合物攝入和減重中獲得了顯著好處,即大大改善了糖尿病控制。也許這次審計最重要的信息是,臨床益處並不取決於達到緩解。
Norwood診所的2型糖尿病緩解率自2017年以來每年都在提高,如表3所示。我們變得越來越有效。這是為什麼呢?我們相信提供更美好未來的希望是必要的,再加上由支持型同伴和專業人士傳達的清晰信息。誠實的反饋是必不可少的跟進。一個非常有用的激勵技巧是向我們的患者提供飲食改變作為終身服藥的替代選擇。有趣的是,當提供這種選擇時,在8年中沒有一個人選擇終身服藥,而是重新努力改善飲食。
77%選擇在診斷後的第一年嘗試低碳水化合物計劃的人達到了緩解,如圖4所示。我們的數據清楚地顯示,緩解的最佳機會在於患有2型糖尿病時間最短的人,這與之前的觀察一致。第一年之後,緩解率下降,表明那些等待更久的人錯過了重要的機會窗口。我們應該關注「代謝年齡」(2型糖尿病的持續時間)而不是實際年齡。我們發現那些達到緩解的人起始時HbA1c較低。這可能是預料之中的,但對於起始時HbA1c較高的人來說仍有希望。起始時HbA1c最高的人在減少飲食碳水化合物後最有可能看到HbA1c的最大改善,如圖4所示(儘管有五名患者在起始HbA1c>90毫摩/升的情況下達到了緩解)。這給了那些控制不良的2型糖尿病患者希望,他們更有可能實現顯著的減輕而不是緩解,並避免服用藥物。最後,從圖4可以看出,選擇低碳水化合物方法的183位參與者中,只有5人(3%)記錄了惡化的HbA1c結果。
減重在緩解中的作用是重要的。我們的發現支持這一點,沒有人在不減重的情況下達到緩解。患者常報告的一個發現是,他們對於在這種飲食下不感到餓感到驚訝。有趣的是,隨機對照試驗已經顯示,低碳水化合物飲食可能既增加能量消耗又降低食慾,這會使減重更加容易。揭示緩解背後生理變化的研究表明,與減重相關的肝脂肪含量顯著減少。在一系列表面上無肝病的初級保健人群中,肝脂肪從非常高的16.0%降至僅3.1%。這完全扭轉了導致空腹高血糖的肝胰島素抗性。它還導致了肝臟向包括胰腺在內的異位部位輸出的甘油三酯大幅減少。胰腺脂肪供應的減少有助於減輕引起β細胞功能障礙的代謝壓力。減重可以通過任何方式引起緩解。其他緩解研究使用了相對高碳水化合物、低熱量的方法,並且食物為基礎的方法或胃旁路手術的臨床研究都實現了緩解。問題是哪種方法對患者來說既安全又有效且最容易被接受?目前的數據顯示了一種在初級保健中非常有效的方法,可以持續避免體重恢復。在一項對篩查出的2型糖尿病成人的研究中,疾病初期體重減少≥10%與5年內緩解率翻倍有關。
2型糖尿病藥物治療成本的上升引起了極大的關注,特別是在老齡化人口和肥胖病流行的情況下。因此,這次審計中記錄的可觀的處方節省具有深遠的重要性。很明顯,許多2型糖尿病患者特別是那些病程較長的人將需要藥物治療。然而,英國國家衛生和護理優質指南關於2型糖尿病的重點更多在於藥物,而對飲食關注甚少。大多數疾病的管理基於對病理生理學的了解,但這種對2型糖尿病性質的新理解尚未納入此類指南。英國國家衛生服務(NHS)英格蘭糖尿病緩解計劃正引導這一變化。2型糖尿病的處方成本可以實現重大的全國節省。同樣重要的是要意識到一些藥物的潛在風險。SGLT2抑製劑可能導致潛在致命的酮症酸中毒。線上補充文件1中包含了一個實用的總結,醫生/護士方案。
這類基於實踐的服務評估普遍存在局限性。缺乏隨機化引入了選擇偏見的風險,因為那些最不積極恢復健康的人不太可能開始這個計劃。鑑於平均基線HbA1c較高(63毫摩/升),不太可能有“挑選最佳案例”的情況。缺乏對照組意味著我們不能直接將這種飲食干預與常規護理進行比較。我們承認存在報告偏見的風險,因為我們依賴每個人關於飲食遵循的話,然而,平均體重減輕10公斤表明有顯著的飲食變化。我們不能確定改變的確切性質或參與者飲食中不同大量營養素的平衡。平均改善的幅度以及這個病例組佔英國NHS診所已知的2型糖尿病病例登記的大比例(39%)(診所有9800名患者)是令人鼓舞的,同樣令人鼓舞的是觀察到這種方法已被證明能幫助英國其他全科診所的2型糖尿病患者。
結論
僅在英格蘭,2020-2021年全國糖尿病審計數據發布證實,超過一百萬人的2型糖尿病控制不佳,HbA1c >58毫摩/升。這對於死亡率具有重要影響,因為英國全國糖尿病審計和國家統計局估計,每年HbA1c >58毫摩/升會使患者失去約100天的壽命。必須找到解決這個問題的新方法,因為英國NHS的常規護理顯然不足。在這種背景下,我們的病例組將平均HbA1c從63毫摩/升改善到46毫摩/升。Norwood診所已經支持2型糖尿病患者減少飲食碳水化合物並減重超過8年。這實現了HbA1c的顯著改善,診所人群中有20%達到了無需藥物的2型糖尿病緩解。還有一系列重要的心血管風險因素改善。與當地平均水平相比,糖尿病藥物節省每年為68,353英鎊。這些節省可能會因減少2型糖尿病的併發症和工作日損失而顯得微不足道。我們的發現顯示,低碳水化合物干預配合減重在為那些HbA1c較低或糖尿病持續時間較短的人提供緩解方面特別有效。它還可以給那些控制不佳的2型糖尿病患者帶來希望,他們在HbA1c上取得了最大的改善。
參考文獻
↵ Brown A , McArdle P , Taplin J , et al . Dietary strategies for remission of type 2 diabetes: a narrative review. J Hum Nutr Diet 2022;35:165–78.doi:10.1111/jhn.12938 pmid:http://www.ncbi.nlm.nih.gov/pubmed/34323335 PubMedGoogle Scholar
↵ Korsmo-Haugen H-K , Brurberg KG , Mann J , et al . Carbohydrate quantity in the dietary management of type 2 diabetes: a systematic review and meta-analysis. Diabetes Obes Metab 2019;21:15–27.doi:10.1111/dom.13499 pmid:http://www.ncbi.nlm.nih.gov/pubmed/30098129 CrossRefPubMedGoogle Scholar
↵ Sainsbury E , Kizirian NV , Partridge SR , et al . Effect of dietary carbohydrate restriction on glycemic control in adults with diabetes: a systematic review and meta-analysis. Diabetes Res Clin Pract 2018;139:239–52.doi:10.1016/j.diabres.2018.02.026 pmid:http://www.ncbi.nlm.nih.gov/pubmed/29522789 CrossRefPubMedGoogle Scholar
↵ Lim EL , Hollingsworth KG , Aribisala BS , et al . Reversal of type 2 diabetes: normalisation of beta cell function in association with decreased pancreas and liver triacylglycerol. Diabetologia 2011;54:2506–14.doi:10.1007/s00125-011-2204-7 pmid:http://www.ncbi.nlm.nih.gov/pubmed/21656330 CrossRefPubMedWeb of ScienceGoogle Scholar
↵ Taylor R , Al-Mrabeh A , Sattar N . Understanding the mechanisms of reversal of type 2 diabetes. Lancet Diabetes Endocrinol 2019;7:726–36.doi:10.1016/S2213-8587(19)30076-2 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31097391 PubMedGoogle Scholar
↵ Lean ME , Leslie WS , Barnes AC , et al . Primary care-led weight management for remission of type 2 diabetes (direct): an open-label, cluster-randomised trial. Lancet 2018;391:541–51.doi:10.1016/S0140-6736(17)33102-1 pmid:http://www.ncbi.nlm.nih.gov/pubmed/29221645 CrossRefPubMedGoogle Scholar
↵ Hallberg SJ , McKenzie AL , Williams PT , et al . Effectiveness and safety of a novel care model for the management of type 2 diabetes at 1 year: an open-label, non-randomized, controlled study. Diabetes Ther 2018;9:583–612.doi:10.1007/s13300-018-0373-9 pmid:http://www.ncbi.nlm.nih.gov/pubmed/29417495 CrossRefPubMedGoogle Scholar
↵ Riddle MC , Cefalu WT , Evans PH , et al . Consensus report: definition and interpretation of remission in type 2 diabetes. Diabetologia 2021;64:2359–66.doi:10.1007/s00125-021-05542-z pmid:http://www.ncbi.nlm.nih.gov/pubmed/34458934 PubMedGoogle Scholar
↵ Unwin D , Unwin J . Low carbohydrate diet to achieve weight loss and improve HbA 1c in type 2 diabetes and pre-diabetes: experience from one general practice. Practical Diabetes 2014;31:76–9.doi:10.1002/pdi.1835 CrossRefGoogle Scholar
↵ Unwin D , Khalid AA , Unwin J , et al . Insights from a general practice service evaluation supporting a lower carbohydrate diet in patients with type 2 diabetes mellitus and prediabetes: a secondary analysis of routine clinic data including HbA1c, weight and prescribing over 6 years. BMJ Nutr Prev Health 2020;3:285–94.doi:10.1136/bmjnph-2020-000072 pmid:http://www.ncbi.nlm.nih.gov/pubmed/33521540 PubMedGoogle Scholar
↵ Unwin DJ , Tobin SD , Murray SW , et al . Substantial and sustained improvements in blood pressure, weight and lipid profiles from a carbohydrate restricted diet: an observational study of insulin resistant patients in primary care. Int J Environ Res Public Health 2019;16:2680.doi:10.3390/ijerph16152680 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31357547 PubMedGoogle Scholar
↵ Unwin D , Unwin J , Crocombe D , et al . Renal function in patients following a low carbohydrate diet for type 2 diabetes: a review of the literature and analysis of routine clinical data from a primary care service over 7 years. Curr Opin Endocrinol Diabetes Obes 2021;28:469–79.doi:10.1097/MED.0000000000000658 pmid:http://www.ncbi.nlm.nih.gov/pubmed/34468402 PubMedGoogle Scholar
↵ Unwin JD , Cuthbertson DJ , Feinman R . A pilot study to explore the role of a lowcarbohydrate intervention to improve GGT levels and HbA1c. Diabesity in practice 2015.Google Scholar
↵ Battelino T , Danne T , Bergenstal RM , et al . Clinical targets for continuous glucose monitoring data interpretation: recommendations from the International consensus on time in range. Diabetes Care 2019;42:1593–603.doi:10.2337/dci19-0028 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31177185 Abstract/FREE Full TextGoogle Scholar
↵ Unwin D , Lake I . An e-learning course on type 2 diabetes and the low Gi diet., in RCGP; 2018.Google Scholar
↵ Gordon EL , Ariel-Donges AH , Bauman V , et al . What Is the evidence for “food addiction?” a systematic review. Nutrients 2018;10:477.doi:10.3390/nu10040477 pmid:http://www.ncbi.nlm.nih.gov/pubmed/29649120 PubMedGoogle Scholar
↵ Unwin D UJ . A simple model to find patient hope for positive lifestyle changes: GRIN.Unwin D,Unwin J.Journal of holistic healthcare Volume 16 Issue 2 Summer 2019. Journal of holistic healthcare 2019;16.Google Scholar
↵ Taylor R , Ramachandran A , Yancy WS , et al . Nutritional basis of type 2 diabetes remission. BMJ 2021;374:n1449.doi:10.1136/bmj.n1449 pmid:http://www.ncbi.nlm.nih.gov/pubmed/34233884 FREE Full TextGoogle Scholar
↵ Schulte EM , Avena NM , Gearhardt AN . Which foods may be addictive? the roles of processing, fat content, and glycemic load. PLoS One 2015;10:e0117959.doi:10.1371/journal.pone.0117959 pmid:http://www.ncbi.nlm.nih.gov/pubmed/25692302 CrossRefPubMedGoogle Scholar
↵ Taylor R , Al-Mrabeh A , Sattar N . Understanding the mechanisms of reversal of type 2 diabetes. Lancet Diabetes Endocrinol 2019.doi:10.1016/S2213-8587(19)30076-2 Google Scholar
↵ Rehackova L , Araújo-Soares V , Steven S , et al . Behaviour change during dietary type 2 diabetes remission: a longitudinal qualitative evaluation of an intervention using a very low energy diet. Diabet Med 2020;37:953–62.doi:10.1111/dme.14066 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31269276 CrossRefPubMedGoogle Scholar
↵ Rehackova L , Araújo-Soares V , Adamson AJ , et al . Acceptability of a very-low-energy diet in type 2 diabetes: patient experiences and behaviour regulation. Diabet Med 2017;34:1554–67.doi:10.1111/dme.13426 pmid:http://www.ncbi.nlm.nih.gov/pubmed/28727247 CrossRefPubMedGoogle Scholar
↵ Steven S , Hollingsworth KG , Al-Mrabeh A , et al . Very low-calorie diet and 6 months of weight stability in type 2 diabetes: pathophysiological changes in responders and nonresponders. Diabetes Care 2016;39:808–15.doi:10.2337/dc15-1942 pmid:http://www.ncbi.nlm.nih.gov/pubmed/27002059 Abstract/FREE Full TextGoogle Scholar
↵ Taylor R , Al-Mrabeh A , Zhyzhneuskaya S , et al . Remission of human type 2 diabetes requires decrease in liver and pancreas fat content but is dependent upon capacity for β cell recovery. Cell Metab 2018;28:547–56.doi:10.1016/j.cmet.2018.07.003 pmid:http://www.ncbi.nlm.nih.gov/pubmed/30078554 CrossRefPubMedGoogle Scholar
↵ Panunzi S , Carlsson L , De Gaetano A , et al . Determinants of diabetes remission and glycemic control after bariatric surgery. Diabetes Care 2016;39:166–74.doi:10.2337/dc15-0575 pmid:http://www.ncbi.nlm.nih.gov/pubmed/26628418 Abstract/FREE Full TextGoogle Scholar
↵ Taylor R . Type 2 diabetes and remission: practical management guided by pathophysiology. J Intern Med 2021;289:754–70.doi:10.1111/joim.13214 pmid:http://www.ncbi.nlm.nih.gov/pubmed/33289165 PubMedGoogle Scholar
↵ Ebbeling CB , Feldman HA , Klein GL , et al . Effects of a low carbohydrate diet on energy expenditure during weight loss maintenance: randomized trial. BMJ 2018;363:k4583.doi:10.1136/bmj.k4583 pmid:http://www.ncbi.nlm.nih.gov/pubmed/30429127 Abstract/FREE Full TextGoogle Scholar
↵ Hu T , Yao L , Reynolds K , et al . The effects of a low-carbohydrate diet on appetite: a randomized controlled trial. Nutr Metab Cardiovasc Dis 2016;26:476–88.doi:10.1016/j.numecd.2015.11.011 pmid:http://www.ncbi.nlm.nih.gov/pubmed/26803589 PubMedGoogle Scholar
↵ Zhyzhneuskaya SV , Al-Mrabeh A , Peters C , et al . Time course of normalization of functional β-cell capacity in the diabetes remission clinical trial after weight loss in type 2 diabetes. Diabetes Care 2020;43:813–20.doi:10.2337/dc19-0371 pmid:http://www.ncbi.nlm.nih.gov/pubmed/32060017 Abstract/FREE Full TextGoogle Scholar
↵ Steven S , Lim EL , Taylor R . Population response to information on reversibility of type 2 diabetes. Diabet Med 2013;30:e135–8.doi:10.1111/dme.12116 pmid:http://www.ncbi.nlm.nih.gov/pubmed/23320491 CrossRefPubMedGoogle Scholar
↵ Dambha-Miller H , Day AJ , Strelitz J , et al . Behaviour change, weight loss and remission of type 2 diabetes: a community-based prospective cohort study. Diabet Med 2020;37:681–8.doi:10.1111/dme.14122 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31479535 PubMedGoogle Scholar
↵NICE. Type 2 diabetes in adults: management, 2022. Available: https://www.nice.org.uk/guidance/ng28 [Accessed 31 Dec 2022].Google Scholar
↵ England N . Low calorie diets to treat obesity and type 2 diabetes, 2019. Available: https://www.england.nhs.uk/diabetes/treatment-care/low-calorie-diets/ Google Scholar
↵ Murdoch C , Unwin D , Cavan D , et al . Adapting diabetes medication for low carbohydrate management of type 2 diabetes: a practical guide. Br J Gen Pract 2019;69:360–1.doi:10.3399/bjgp19X704525 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31249097 FREE Full TextGoogle Scholar
↵ Morris E , Aveyard P , Dyson P , et al . A food-based, low-energy, low-carbohydrate diet for people with type 2 diabetes in primary care: a randomized controlled feasibility trial. Diabetes Obes Metab 2020;22:512–20.doi:10.1111/dom.13915 pmid:http://www.ncbi.nlm.nih.gov/pubmed/31709697 CrossRefPubMedGoogle Scholar
↵ Oliver D , Andrews K . Brief intervention of low carbohydrate dietary advice: clinic results and a review of the literature. Curr Opin Endocrinol Diabetes Obes 2021;28:496–502.doi:10.1097/MED.0000000000000665 pmid:http://www.ncbi.nlm.nih.gov/pubmed/34310366 PubMedGoogle Scholar
↵National diabetes audit 2020-21 data release, 2021. England. Available: https://digital.nhs.uk/data-and-information/publications/statistical/national-diabetes-audit Google Scholar
↵ Heald AH , Stedman M , Davies M , et al . Estimating life years lost to diabetes: outcomes from analysis of national diabetes audit and office of national statistics data. Cardiovasc Endocrinol Metab 2020;9:183–5.doi:10.1097/XCE.0000000000000210 pmid:http://www.ncbi.nlm.nih.gov/pubmed/33225235 PubMedGoogle Scholar
McCombie L , Leslie W , Taylor R , et al . Beating type 2 diabetes into remission. BMJ 2017;358:j4030.doi:10.1136/bmj.j4030 pmid:http://www.ncbi.nlm.nih.gov/pubmed/28903916 FREE Full TextGoogle Scholar



 English
English Bahasa Melayu
Bahasa Melayu Bahasa Indonesia
Bahasa Indonesia Tiếng Việt
Tiếng Việt ไทย
ไทย