本翻譯僅作學術交流用,無商業意圖,請勿轉載,如有疑議問請來信
最新共識報告對第2型糖尿病的緩解提出新定義。研究顯示,透過醫療干預,部分患者血糖水平可恢復正常,甚至在停止降糖藥物治療後仍持續改善。此報告由國際專家組提出,旨在為未來臨床指南奠定基礎,改善對糖尿病緩解的理解與處理。

共識報告:第2型糖尿病緩解的定義與詮釋
Consensus Report: Definition and Interpretation of Remission in Type 2 Diabetes
Matthew C. Riddle, William T. Cefalu, Philip H. Evans, Hertzel C. Gerstein, Michael A. Nauck, William K. Oh, Amy E. Rothberg, Carel W. le Roux, Francesco Rubino, Philip Schauer, Roy Taylor, Douglas Twenefour; Consensus Report: Definition and Interpretation of Remission in Type 2 Diabetes. Diabetes Care 1 October 2021; 44 (10): 2438–2444.
Abstract
Improvement of glucose levels into the normal range can occur in some people living with diabetes, either spontaneously or after medical interventions, and in some cases can persist after withdrawal of glucose-lowering pharmacotherapy. Such sustained improvement may now be occurring more often due to newer forms of treatment. However, terminology for describing this process and objective measures for defining it are not well established, and the long-term risks versus benefits of its attainment are not well understood. To update prior discussions of this issue, an international expert group was convened by the American Diabetes Association to propose nomenclature and principles for data collection and analysis, with the goal of establishing a base of information to support future clinical guidance. This group proposed “remission” as the most appropriate descriptive term, and HbA1c <6.5% (48 mmol/mol) measured at least 3 months after cessation of glucose-lowering pharmacotherapy as the usual diagnostic criterion. The group also made suggestions for active observation of individuals experiencing a remission and discussed further questions and unmet needs regarding predictors and outcomes of remission.
摘要
一些糖尿病患者的血糖水平可以自然或經過醫療干預進入正常範圍,在某些情況下,即使停止降糖藥物治療後也能持續改善。由於新型治療方式的出現,這種持續的改善現在可能更為常見。然而,描述這一過程的術語和定義它的客觀測量標準尚未確立,其長期風險與效益的理解也不充分。為了更新以往對這一問題的討論,美國糖尿病協會召集了一個國際專家小組,提出了命名和資料收集分析原則,目的是建立一個資訊基礎,以支持未來的臨床指導。該小組提出使用“緩解”作為最合適的描述術語,並將HbA1c<6.5%(48毫摩爾/摩爾)作為停止降糖藥物治療至少3個月後的通常診斷標準。該小組還就積極觀察經歷緩解的個體提出了建議,並討論了關於緩解的預測因子和結果的進一步問題與未滿足的需求。
第2型糖尿病(T2D)的自然歷史現在比以前更被了解。它顯然是異質的,遺傳和環境因素均對其發病機制和演變有所貢獻。通常,遺傳易感性在出生時就存在,但定義糖尿病的高血糖只是逐漸出現,並在成年期達到診斷水平。調節T2D表現的環境因素包括各種食物的可獲得性;體育活動的機會和參與;與家庭、工作或其他影響相關的壓力;暴露於污染物和毒素;以及公共衛生和醫療資源的獲取。兩種常見但暫時性的事件可能導致易感個體較早出現高血糖:懷孕或短期糖皮質激素治療。因此,人們可能發展出“妊娠糖尿病”或“類固醇糖尿病”,這些狀況雖然與典型T2D有所不同,但仍與其相關(1,2)。在這些情況下,高血糖是由胰島素抵抗引起的,但可能不會持續,因為當嬰兒出生或類固醇治療結束時,對胰島素的反應會改善。懷孕後血糖水平可能恢復正常,但後來發展成T2D的風險仍然增加(3)。急性疾病或其他壓力大的經歷也可能在易感個體中引發暫時性高血糖,有時稱為“壓力性高血糖”。逐漸發展且獨立於這些刺激的T2D,最常伴隨中年體重增加,有時在減重後可以更容易控制或似乎緩解。此外,T2D患者可能因病、情緒困擾或與嚴重社會動盪相關的食物短缺而無意間減輕體重。在T2D中,體重的自願或意外下降可能允許或要求停止降糖治療。
這些血糖模式的變化對流行病學具有重要意義。其中一點是,在某些情況下,T2D可以在沒有特定干預的情況下緩解。另一點是,特定於糖尿病的併發症,如糖尿病性腎小球病變,可以在過去曾暴露於慢性高血糖的非同時期糖尿病患者中發現(4)。還有一點是T2D中血糖水平與死亡率之間存在U型關係,即在正常或較低的血紅蛋白A1c(HbA1c)水平下風險增加。這種模式可能歸因於T2D的過度治療,導致低血糖風險增加(5),但另一方面可能是由於體重減輕和血糖水平下降是由於另一種嚴重且可能致命的疾病(6)。因此,血糖水平的持續增加和持續下降都可能自然發生或通過干預而發生,並可能引起解釋上的問題。
近年來,針對T2D的代謝控制治療有了很大改進。在成人首次出現T2D時進行短期藥物治療有時可以恢復接近正常的血糖控制,從而允許撤回治療(7-9)。伴隨血糖控制恢復的“血糖毒性”逆轉在早期強化胰島素治療中有最好的記錄,但也可以通過其他干預發生。新類藥物,即類似胰高血糖素1(GLP-1)受體激動劑和鈉-葡萄糖共轉運蛋白抑製劑,有時可以達到極好的血糖控制,且很少導致低血糖。顯著的行為改變 – 主要與營養和體重管理有關 – 可以導致從明顯高血糖回到幾乎正常的血糖水平,並持續相當長的時間(10,11)。更戲劇性的是,外科或其他腸道干預可以通過其他機制誘導顯著的體重減輕和代謝控制的進一步改善,並持續相當長的時間(12-14)- 在某些情況下為5年或更長。在所有這些形式的干預之後,早期T2D病程中最有可能恢復幾乎正常的血糖調節,並可能涉及胰島素分泌和胰島素作用的部分恢復(15)。
日益增長的將血糖水平持續改善至正常範圍的經驗,促使人們重新評估可能指導當前討論和未來研究的術語和定義,這些研究涉及T2D中血糖轉變的管理。2009年,由美國糖尿病協會(ADA)發起的一份共識聲明就這些問題進行了探討(16)。它建議將“緩解”作為描述性術語,意指“徵狀和症狀的緩解或消失”。提出了三種緩解類別。“部分”緩解被認為發生在至少1年內維持低於糖尿病診斷閾值的高血糖,且不進行主動藥物治療。“完全”緩解被描述為1年內不用藥物治療就能維持正常的血糖水平。“長期”緩解可以描述為完全緩解持續5年或以上,且不需藥物治療。HbA1c<6.5%(<48毫摩爾/摩爾)和/或空腹血漿葡萄糖(FPG)100–125 mg/dL(5.6至6.9毫摩爾/升)用於定義部分緩解,而完全緩解則要求HbA1c和FPG的“正常”水平(<100 mg/dL [5.6毫摩爾/升])。
為了在更近期的經驗背景下擴展此聲明和後續出版物(17),ADA召集了一個國際的、多學科的專家小組。來自美國糖尿病協會、歐洲糖尿病研究協會、英國糖尿病協會、內分泌學會和糖尿病手術峰會的代表都包括在內。為了提供另一種觀點,一位腫瘤學家也是專家小組的一部分。該小組於2019年2月至2020年9月期間進行了三次面對面會議,並在此期間進行了額外的電子交流。以下是這些討論和從中得出的結論的總結。本報告並非旨在制定治療指南或偏好特定干預。相反,基於作者達成的共識,它提出了適當的術語定義和評估血糖測量的方法,以促進數據的收集和分析,這可能導致未來的臨床指導。
最佳術語
術語的選擇對臨床實踐和政策決策有影響。對於已經擺脫先前診斷疾病狀態的人,提出了幾個術語。在第2型糖尿病(T2D)中,解決、逆轉、緩解和治愈等術語均被用來描述干預導致無病狀態的有利結果。與先前共識小組的結論(16)一致,這個專家小組得出結論認為糖尿病緩解是最合適的術語。它達到了適當的平衡,指出糖尿病可能不總是處於活躍和進展狀態,但暗示顯著改善可能不是永久性的。這與認為一個人可能需要持續的支持以避免復發,並需要定期監測以允許在高血糖再次發生時進行干預的觀點一致。緩解是腫瘤學領域廣泛使用的術語(18),定義為癌症徵狀和症狀的減少或消失。
一個常見的傾向是將緩解等同於“無疾病證據”,允許二元選擇的診斷。然而,糖尿病是由高血糖定義的,而高血糖存在於一個連續體上。共識小組得出結論認為,“無糖尿病證據”不是適用於T2D的合適術語。做出這一決定的原因之一是,T2D的潛在病理生理學,包括胰島素缺乏和對胰島素作用的抵抗,以及其他異常,很少被干預完全正常化(19-21)。此外,任何用於識別糖尿病緩解的標準必然是任意的,是血糖水平連續體上的一個點。儘管先前的共識聲明建議將糖尿病緩解分為部分和完全兩個類別,使用不同的血糖閾值(16),但這種區分可能會引入影響保險費用、報銷和醫療遭遇編碼相關政策決策的歧義。先前聲明建議的超過5年的長期緩解應單獨考慮,並沒有客觀依據。目前小組懷疑這種區分會幫助臨床決策或流程,至少在關於長期緩解的頻率和與之相關的醫療結果的更客觀信息可用之前是這樣。基於血糖測量的單一緩解定義被認為更有可能有所幫助。
其他候選術語也有其局限性。認為糖尿病診斷已解決,似乎暗示原始診斷有誤,或者一個完全正常的狀態已經永久建立。術語“逆轉”用於描述返回到低於糖尿病診斷閾值的血糖水平的過程,但它不應該與緩解狀態等同。術語“治愈”在暗示病情的所有方面現在已正常化,且不再需要臨床隨訪或進一步管理,無論是對於高血糖的復發還是與潛在生理異常相關的其他風險,這似乎尤其有問題。雖然“治愈”是一個期待的結果,就像癌症患者一樣,小組同意在T2D的背景下應避免使用這個術語。
診斷T2D緩解的血糖標準
廣泛用於T2D診斷或血糖管理的測量包括HbA1c、空腹血漿葡萄糖(FPG)、口服葡萄糖挑戰後2小時的血漿葡萄糖,以及連續血糖監測(CGM)測得的日均血糖。小組偏好於HbA1c低於目前用於初步診斷糖尿病的水平,即6.5%(48毫摩爾/摩爾),並至少持續3個月在這一水平,而無需繼續使用常規降糖藥物,作為主要的定義測量。用於測量HbA1c的方法必須有嚴格的質量保證,並且檢測必須標準化,以符合國際參考值的標準(22-24)。
然而,許多因素可能影響HbA1c的測量,包括變異血紅蛋白、糖化率的不同或紅細胞存活期的改變,這些可以在多種疾病狀態中發生。關於哪些方法受變異血紅蛋白影響的信息可以在 http://ngsp.org/interf.asp 找到。因此,在某些人中,即使血糖實際上升高時,也可能出現正常的HbA1c值,或者當平均血糖正常時HbA1c可能偏高。在HbA1c可能不可靠的情況下,通過CGM測量24小時平均血糖濃度被提出作為一種替代方案。通過CGM觀察到的平均血糖計算得出的糖化血紅蛋白值被稱為估計的HbA1c(eA1C)(25),或最近稱為血糖管理指標(GMI)(26)。在HbA1c值的準確性不確定的情況下,可以使用CGM來評估平均血糖和HbA1c之間的相關性,並識別出正常範圍以外的模式(27,28)。
空腹血漿葡萄糖(FPG)低於126 mg/dL(7.0毫摩爾/升)在某些情況下可作為緩解的另一標準,就像高於該水平的值是T2D初步診斷的另一選擇一樣。這種方法的缺點是需要在經過一夜的空腹後收集樣本,並且重複測量之間存在顯著變異。在75克口服葡萄糖挑戰後測試2小時血漿葡萄糖似乎是一個較不理想的選擇,部分原因是獲得該測試的複雜性較高,且重複測量之間的變異性很高。此外,代謝外科手術干預可能會改變口服葡萄糖挑戰後血糖反應的通常模式,表現為早期高血糖後的低血糖,進一步混淆了該測試的解釋。
綜合考慮所有選擇,小組強烈支持在一般情況下使用HbA1c<6.5%(48毫摩爾/摩爾)作為通常可靠且最簡單、最廣為人知的定義標準。在某些情況下,eA1C或GMI<6.5%可以被視為等效標準。
在使用降糖藥物時能否診斷出緩解?
糖尿病緩解可能通過改變生活方式、其他醫療或外科干預,或者經常是這些方法的組合,來實現。在診斷緩解之前是否需要停止治療,這取決於干預方式。涉及營養和體育活動的日常生活方式的改變,其健康效果遠遠超出與糖尿病相關的範疇。此外,不僅實現糖尿病緩解,而且一般改善健康狀況的可能性,可能是個人首先做出這些改變的動機。這些考慮也適用於外科手術方法,此外,外科手術並不容易逆轉。因此,在手術後和持續的生活方式努力中可以診斷出緩解。
在持續的藥物治療背景下能否診斷出緩解,這是一個更複雜的問題。在某些情況下,短期使用一種或多種降糖藥物可以恢復出色的血糖控制,即使在停用這些藥物後,幾乎正常的血糖水平仍然持續。如果持續使用降糖藥物治療,則無法辨別是否發生了藥物獨立的緩解。只有在所有降糖藥物停用一段時間後,才能診斷出緩解,這段時間既足夠讓藥物的效果減弱,也足以評估藥物缺席對HbA1c值的影響。
這一標準適用於所有降糖藥物,包括那些具有其他效果的藥物。值得注意的是,可能會開處方用美托福明來維持體重、改善心血管疾病或癌症風險標記,或治療多囊卵巢綜合症(29)。GLP-1受體激動劑可能被優先用於控制體重或降低心血管事件的風險,而鈉-葡萄糖共轉運蛋白抑制劑可能被開處方用於心力衰竭或腎保護。如果這些考慮排除了停用這些藥物的可能性,那麼即使維持幾乎正常的血糖水平,也不能診斷出緩解。臨床決策可能會決定繼續這些治療而不檢測緩解,而在這種情況下,是否真正達到了緩解仍然是未知的。小組還認識到,一些藥物具有適度的降糖效果,但並非用於降糖,就像某些減肥藥物的情況一樣。由於這些藥物不是專門用於管理高血糖,因此在診斷糖尿病緩解之前不需要停用它們。
另一個關注點是預防性藥物干預在已被診斷為緩解的個體或其他已知具有非常高T2D風險的人群中的可能作用,例如有過妊娠糖尿病歷史的婦女。這些人是否應該成為使用降糖治療的候選者,特別是使用美托福明?這是一個有爭議的領域,既有支持也有反對的論點。支持藥物治療以防止明顯糖尿病的出現或再次出現的是,有可能安全且經濟地消除未診斷但有害的高血糖時期(30)。另一方面的論點是,藥物治療對β細胞惡化的保護尚未令人信服地被證明,且預防性干預有已知的成本和潛在風險(31)。
這份聲明認為,是否對預防性干預進行正當化超出了目前聲明的範圍,除了指出,如果使用預防性干預,則無法知道緩解是否持續。基於本文件所提出的定義系統性地收集的數據可能有助於澄清在此背景下可能使用的各種干預的角色。
診斷緩解的時間方面
當T2D的干預是通過藥物治療或手術時,開始的時間容易確定,臨床效果迅速顯現(表1)。當干預是通過改變生活方式時,效益的開始可能較慢,可能需要長達6個月的時間來穩定效果。另一個時間因素是,有效干預完全反映在HbA1c的變化上所需的大約3個月時間,HbA1c反映了幾個月期間的平均血糖水平。考慮到這些因素,在開始生活方式干預後至少需要6個月的時間,才能通過測試HbA1c可靠地評估反應。在更迅速有效的外科手術干預之後,需要至少3個月的時間讓HbA1c值穩定。當干預是臨時藥物治療,或者當生活方式或代謝手術干預添加到先前的藥物治療時,需要至少3個月的時間,在停用任何降糖藥物後。對於所有導致緩解的干預,建議後續測量HbA1c的頻率不要超過每3個月,也不要少於每年一次,以確認緩解的持續。與HbA1c不同,FPG或從CGM衍生的eA1C在干預開始後的較短時間內就可以穩定,或者如果血糖控制後來惡化,則可以更快增加。當這些血糖測量替代HbA1c時,可以在干預後較早收集並隨後更頻繁進行,但由於它們更易變化,符合緩解開始或失去的值應通過重複測量來確認。
表1確定T2D緩解的干預和時間因素
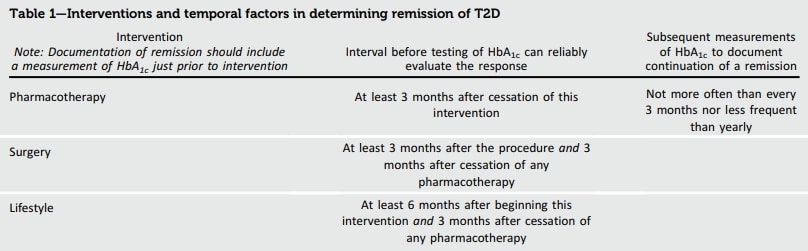
藥物治療、生活方式或代謝手術干預後緩解的生理學考慮
當在使用臨時降糖藥物後記錄到緩解時,藥物治療的直接效果並不持續。逆轉由於代謝控制不良(32)對胰島素分泌和作用的不利影響可能建立了一個緩解,但其他潛在的異常持續存在,緩解的持續時間相當可變。相反,當持續的生活方式變化導致緩解時,食物攝入、體力活動以及壓力和環境因素的管理變化可以長時間有利地改變胰島素分泌和作用。在這種情況下,長期緩解是可能的,但不是肯定的。代謝手術的影響更深刻且通常更持久(33)。胃腸道的結構變化導致了一種新的激素環境。這包括在進食後血液中GLP-1濃度增加數倍等變化,這些變化通過與大腦相關區域的互動可能會減少食慾和食物攝入,並額外改變周邊代謝。這些機制重新建立的血糖恆定通常持續時間更長。解剖學和生理學的變化基本上是永久的,但即便如此,對血糖模式的理想效果可能無法無限期地持續。部分體重恢復可能發生,且β細胞能力的持續下降可能會隨時間推移導致血糖水平上升。
持續監測
正如剛才所描述的,緩解是一種糖尿病不存在但仍需持續觀察的狀態,因為高血糖經常會復發。體重增加、其他形式疾病的壓力,以及β細胞功能的持續下降都可能導致T2D復發。應至少每年進行一次HbA1c或其他血糖控制測量。需要持續關注保持健康的生活方式,並避免使用已知促進高血糖的藥物來治療其他狀況,特別是糖皮質激素和某些抗精神病藥物。
在這種情況下,代謝記憶或遺留效應(34)是相關的。這些術語描述了先前高血糖在各種組織中持續的有害效果。即使在緩解後,糖尿病的典型並發症 – 包括視網膜病變、腎病變、神經病變和心血管疾病風險增加 – 仍然可能發生(35)。因此,應建議從糖尿病緩解的人定期進行視網膜檢查、腎功能測試、足部評估,以及血壓和體重測量,除了持續監測HbA1c之外。目前還沒有長期證據表明,通常建議的並發症評估可以安全地停止。應建議處於緩解狀態的個體繼續接受積極的醫學觀察,包括定期檢查。
除了T2D已建立的並發症的持續逐漸進展外,緩解可能還與另一種風險相關。這是在長期高血糖後血糖水平迅速降低時,微血管疾病突然惡化的可能性。特別是,當存在較差的血糖控制以及視網膜病變超出微動脈瘤存在時,應避免迅速降低血糖水平,如果觀察到血糖迅速下降,應重複進行視網膜檢查。這個建議主要基於胰島素治療開始或加強後視網膜病變惡化的經驗,這種情況只有在基線時存在中度或更嚴重的視網膜病變時才會出現(36,37)。其他干預措施也可能導致視網膜病變惡化,儘管有一些證據表明代謝手術後這種風險較小(38)。
進一步的問題和未滿足的需求
前述討論主要基於專家意見。它並非旨在提供有關如何或何時尋求符合緩解標準的血糖控制的指導。它也不旨在澄清在識別出緩解後預防性藥物治療的角色。相反,它提出了術語和結構,以促進未來的研究和收集信息,以支持未來的臨床指南。以下列出了一些需要進一步研究的領域。
驗證使用6.5% HbA1c作為定義測量的有效性
使用6.5% HbA1c(48毫摩爾/摩爾)作為診斷緩解的切點,與使用6.0% HbA1c(42毫摩爾/摩爾)、HbA1c 5.7%(39毫摩爾/摩爾)或其他水平,在預測復發風險或微血管或心血管並發症的相對有效性應進行評估。應進一步探索使用CGM衍生數據調整HbA1c目標範圍以識別血糖緩解。可以研究使用與HbA1c <6.5%(<48毫摩爾/摩爾)相當的CGM衍生平均血糖,或使用FPG <7.0毫摩爾/升(<126 mg/dL)代替HbA1c。
血糖測量時間的驗證
可能在不改變預測效率的情況下,減少HbA1c的測試頻率。例如,6個月和12個月的常規測量可能足以在短期內識別緩解和復發風險。
評估緩解確立後美托福明和其他藥物的效果
美托福明影響糖尿病血糖控制的主要作用是改善肝臟對門靜脈胰島素的反應性。它是否能通過其他機制延遲復發尚不清楚。在診斷緩解後,使用美托福明或其他非用於血糖指徵的藥物可能會延遲高血糖的復發和/或保護免受其他代謝紊亂的進展。關於這一點的客觀信息有限,顯然需要更多的研究。
評估緩解期間的非血糖指標
改善的血糖控制不是可能影響長期結果的唯一代謝方面。例如,循環脂蛋白質檔案、周邊和內臟脂肪,以及肝臟和其他組織中的細胞內脂肪沉積可能都是伴隨血糖緩解出現的相關效應,或可能與血糖緩解分開,這些都可以進行評估。藥物、行為或外科干預後GLP-1和其他肽介質變化在改變復發或醫療事件風險方面的作用尚未知。
緩解持續時間的研究
由各種干預引起的緩解預期持續時間仍未明確界定,應更全面地檢查與緩解復發相關的因素。
記錄緩解後的長期結果
緩解對死亡率、心血管事件、功能能力和生活質量的長期影響仍然未知。緩解期間與這些結果相關的代謝和臨床因素理解不足,可以進行界定。
為醫療專業人員和患者開發教育材料
為處於緩解狀態的個體開發和標準化教育和篩查計劃,將有助於將各種建議應用於臨床實踐。
結論
通過使用當前和新興的醫療或生活方式干預措施或代謝手術,典型第2型糖尿病(T2D)患者的血糖水平有時可以恢復到正常或接近正常水平。在這種情況下持續代謝改善的頻率、可能持續的時間,以及其對後續醫療結果的影響仍不清楚。為了促進臨床決策、數據收集和有關結果的研究,需要更清晰的術語來描述這種改善。基於我們的討論,我們提出以下建議:
- 用於描述T2D中持續的代謝改善到接近正常水平的術語應該是糖尿病緩解。
- 緩解應被定義為HbA1c恢復到<6.5%(<48毫摩爾/摩爾),這種情況發生於自然或在某種干預後,並且在沒有常用降糖藥物治療的情況下持續至少3個月。
- 當HbA1c被認定為不可靠的慢性血糖控制標記時,空腹血漿葡萄糖(FPG)<126 mg/dL(<7.0毫摩爾/升)或從CGM值計算出的eA1C<6.5%可以用作替代標準。
- 進行HbA1c檢測以記錄緩解應在干預之前進行,並且在干預開始和停止任何降糖藥物治療後至少3個月後進行。
- 後續測試以確定長期維持緩解應至少每年進行一次,並與常規建議的糖尿病潛在並發症測試一起進行。
- 根據本聲明中概述的術語和定義進行的研究,需要確定使用可用干預措施的T2D緩解的頻率、持續時間和對短期和長期醫療結果的影響。
本共識報告由《臨床內分泌學與代謝雜誌》(由牛津大學出版社代表內分泌學會出版)、《糖尿病學》(由施普林格-維拉格出版社代表歐洲糖尿病研究協會出版)、《糖尿病醫學》(由威利出版社代表英國糖尿病協會出版)和《糖尿病護理》(由美國糖尿病協會出版)聯合發表。
關於特定主題的共識報告包括全面的審查,由專家小組(即共識小組)撰寫,代表該小組的集體分析、評估和意見。當臨床醫生、科學家、監管機構和/或政策制定者希望就與糖尿病相關的醫學或科學問題尋求指導和/或明確性,且證據矛盾、新興或不完整時,就需要共識報告。共識報告還可能強調證據中的空白並提出未來研究的領域以解決這些空白。共識報告不是美國糖尿病協會(ADA)的立場,而只代表專家意見,並在ADA的主持下由受邀專家製作。共識報告可能在ADA臨床會議或研究研討會後開發。
© 2021內分泌學會、歐洲糖尿病研究協會、英國糖尿病協會和美國糖尿病協會。讀者可以使用本文,只要工作被適當引用,使用是教育性的且非盈利的,且工作未被改變。更多信息可在 https://www.diabetesjournals.org/content/license 獲得。
參考文獻
1.Vounzoulaki E, Khunti K, Abner SC, Tan BK, Davies MJ, Gillies CL. Progression to type 2 diabetes in women with a known history of gestational diabetes: systematic review and meta-analysis. BMJ 2020;369:m1361
Google Scholar
2.Simmons LR, Molyneaux L, Yue DK, Chua EL. Steroid-induced diabetes: is it just unmasking of type 2 diabetes? ISRN Endocrinol 2012;2012:910905
Google ScholarCrossref
3.Li Z, Cheng Y, Wang D, et al. Incidence rate of type diabetes mellitus after gestational diabetes mellitus: a systematic review and meta-analysis of 170,139 women. J Diab Res 2020;3076463
Google Scholar
4.Selvin E, Ning Y, Steffes MW, et al. Glycated hemoglobin and the risk of kidney disease and retinopathy in adults with and without diabetes. Diabetes 2011;60:298–305
Google ScholarCrossref
5.Currie CJ, Peters JR, Tynan A, et al. Survival as a function of HbA1c in people with type 2 diabetes: a retrospective cohort study. Lancet 2010;375:481–489
Google ScholarCrossref
6.Carson AP, Fox CS, McGuire DK, et al. Low hemoglobin A1c and risk of all-cause mortality among US adults without diabetes. Circ Cardiovasc Qual Outcomes 2010;3:661–667
Google ScholarCrossref
7.Kramer CK, Zinman B, Retnakaran R. Short-term intensive insulin therapy in type 2 diabetes mellitus: a systematic review and meta-analysis. Lancet Diabetes Endocrinol 2013;1:28–34
Google ScholarCrossref
8.Kramer CK, Zinman B, Choi H, Retnakaran R. Predictors of sustained drug-free diabetes remission over 48 weeks following short-term intensive insulin therapy in early type 2 diabetes. BMJ Open Diabetes Res Care 2016;4:e000270
Google ScholarCrossref
9.McInnes N, Smith A, Otto R, et al. Piloting a remission strategy in type 2 diabetes: results of a randomized controlled trial. J Clin Endocrinol Metab 2017;102:1596–1605
Google ScholarCrossref
10.Lean MEJ, Leslie WS, Barnes AC, et al. Durability of a primary care-led weight-management intervention for remission of type 2 diabetes: 2-year results of the DiRECT open-label, cluster-randomised trial. Lancet Diabetes Endocrinol 2019;7:344–355
Google ScholarCrossref
11.Gregg EW, Chen H, Wagenknecht LE, et al.; Look AHEAD Research Group. Association of an intensive lifestyle intervention with remission of type 2 diabetes. JAMA 2012;308:2489–2496
Google ScholarCrossref
12.Mingrone G, Panunzi S, De Gaetano A, et al. Metabolic surgery versus conventional medical therapy in patients with type 2 diabetes: 10-year follow-up of an open-label, single-centre, randomised controlled trial. Lancet 2021;397:293–304
Google ScholarCrossref
13.Rubino F, Nathan DM, Eckel RH, et al.; Delegates of the 2nd Diabetes Surgery Summit. Metabolic surgery in the treatment algorithm for type 2 diabetes: a joint statement by international diabetes organizations. Diabetes Care 2016;39:861–877
Google ScholarCrossref
14.Schauer PR, Bhatt DL, Kirwan JP, et al.; STAMPEDE Investigators. Bariatric surgery versus intensive medical therapy for diabetes: 5-year outcomes. N Engl J Med 2017;376:641–651
Google ScholarCrossref
15.White MG, Shaw JAM, Taylor R. Type 2 diabetes: the pathologic basis of reversible β-cell dysfunction. Diabetes Care 2016;39:2080–2088
Google ScholarCrossref
16.Buse JB, Caprio S, Cefalu WT, et al. How do we define cure of diabetes? Diabetes Care 2009;32:2133–2135
Google ScholarCrossref
17.Nagi D, Hambling C, Taylor R. Remission of type 2 diabetes: a position statement from the Association of British Clinical Diabetologists (ABCD) and the Primary Care Diabetes Society (PCDS). Br J Diabetes 2019;19:73–76
Google ScholarCrossref
18.Barnes E. Between remission and cure: patients, practitioners and the transformation of leukaemia in the late twentieth century. Chronic Illn 2007;3:253–264
Google ScholarCrossref
19.Taylor R, Al-Mrabeh A, Zhyzhneuskaya S, et al. Remission of human type 2 diabetes requires decrease in liver and pancreas fat content but is dependent upon capacity for β cell recovery. Cell Metab 2018;28:547–556.e3
Google ScholarCrossref
20.Lim EL, Hollingsworth KG, Aribisala BS, Chen MJ, Mathers JC, Taylor R. Reversal of type 2 diabetes: normalisation of beta cell function in association with decreased pancreas and liver triacylglycerol. Diabetologia 2011;54:2506–2514
Google ScholarCrossref
21.Camastra S, Manco M, Mari A, et al. Beta-cell function in severely obese type 2 diabetic patients: long-term effects of bariatric surgery. Diabetes Care 2007;30:1002–1004
Google ScholarCrossref
22.Consensus Committee. Consensus statement on the worldwide standardization of the hemoglobin A1C measurement: the American Diabetes Association, European Association for the Study of Diabetes, International Federation of Clinical Chemistry and Laboratory Medicine, and the International Diabetes Federation. Diabetes Care 2007;30:2399–2400
Crossref
23.Jeppsson J-O, Kobold U, Barr J, et al.; International Federation of Clinical Chemistry and Laboratory Medicine (IFCC). Approved IFCC reference method for the measurement of HbA1c in human blood. Clin Chem Lab Med 2002;40:78–89
Google ScholarCrossref
24.EurA1c Trial Group. EurA1c: the European HbA1c trial to investigate the performance of HbA1c assays in 2166 laboratories across 17 countries and 24 manufacturers by use of the IFCC model for quality targets. Clin Chem 2018;64:1183–1192
Crossref
25.Danne T, Nimri R, Battelino T, et al. Inter-national consensus on use of continuous glucose monitoring. Diabetes Care 2017;40:1631–1640
Google ScholarCrossref
26.Bergenstal RM, Beck RW, Close KL, et al. Glucose management indicator (GMI): a new term for estimating A1C from continuous glucose monitoring. Diabetes Care 2018;41:2275–2280
Google ScholarCrossref
27.Beck RW, Connor CG, Mullen DM, Wesley DM, Bergenstal RM. The fallacy of average: how using HbA1c alone to assess glycemic control can be misleading. Diabetes Care 2017;40:994–999
Google ScholarCrossref
28.Shah VN, DuBose SN, Li Z, et al. Continuous glucose monitoring profiles in healthy nondiabetic participants: a multicenter prospective study. J Clin Endocrinol Metab 2019;104:4356–4364
Google ScholarCrossref
29.Hundal RS, Inzucchi SE, Metformin: new understandings, new uses. Drugs 2003;63:1879–1894
Google ScholarCrossref
30.Herman WH, Ratner RE. Metformin should be used to treat prediabetes in selected individuals. Diabetes Care 2020;43:1988–1990
Google ScholarCrossref
31.Davidson MB. Metformin should not be used to treat prediabetes. Diabetes Care 2020;43:1983–1987
Google ScholarCrossref
32.Yki-Järvinen H. Glucose toxicity. Endocr Rev 1992;13:415–431
Google Scholar
33.Isaman DJ, Rothberg AE, Herman WH. Reconciliation of type 2 diabetes remission rates in studies of Roux-en-Y gastric bypass. Diabetes Care 2016;39:2247–2253
Google ScholarCrossref
34.Ceriello A. The emerging challenge in diabetes: the “metabolic memory.” Vascul Pharmacol 2012;57:133–138
Google ScholarCrossref
35.Murphy R, Jiang Y, Booth M, et al. Progression of diabetic retinopathy after bariatric surgery. Diabet Med 2015;32:1212–1220
Google ScholarCrossref
36.Arun CS, Pandit R, Taylor R. Long-term progression of retinopathy after initiation of insulin therapy in Type 2 diabetes: an observational study. Diabetologia 2004;47:1380–1384
Google ScholarCrossref
37.The Diabetes Control and Complications Trial Research Group. Early worsening of diabetic retinopathy in the Diabetes Control and Complications Trial. Arch Ophthalmol 1998;116:874–886
Crossref
38.Singh RP, Gans R, Kashyap SR, et al. Effect of bariatric surgery versus intensive medical management on diabetic ophthalmic outcomes. Diabetes Care 2015;38:e32–e33
Google ScholarCrossref



 English
English Bahasa Melayu
Bahasa Melayu Bahasa Indonesia
Bahasa Indonesia Tiếng Việt
Tiếng Việt ไทย
ไทย